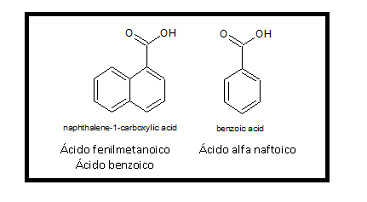
Ácido aromático
| ||||||
Ácido Aromático. Al principio, la palabra aromático se aplicaba a sustancias de olor agradable pero ahora esta palabra describe al benceno, sus derivados y otros compuestos que exhiben propiedades químicas semejantes. En la actualidad la fuente principal de hidrocarburos aromáticos, es la refinación del petróleo. El benceno es el hidrocarburo aromático más sencillo. Su formula molecular es C 6 H 6 Tiene una estructura anular simétrica. Es un líquido incoloro de aroma dulce y sabor ligeramente amargo, similar al de la hiel. Se evapora al aire rápidamente y es poco soluble en agua. Es sumamente inflamable, volátil. Se derivan otros hidrocarburos de este tipo entre los que se encuentran: el tolueno, el orto-xileno, el meta-xileno y el para-xileno, polinucleicos que son el naftaleno, el fenantreno y antraceno
Sumario
Ortoxileno, metaxileno, paraxileno
Los dimetilbenceno se llaman “xilenos” 3 compuestos diferentes tienen la fórmula C 6 H 4 (CH 3) 2
Nomenclatura
Reglas: 1. Si solo hay un grupo en ele anillo, no es necesaria la numeración para establecer su posición 2. Si hay dos grupos en ele anillo, se usa la designación tradicional:
- orto- u- o- para disustitución 1,2
- meta-o- m -para disustitución 1,3
- para-o- p -para disustitución 1,4
3. Si hay tres o más grupos en el anillo se asignan números de tal manera que su suma sea la mínima
- Cuando se elimina un átomo H de una molécula de benceno C6H6 el grupo resultante C6H5-O - - recibe el nombre de fenil(o)
Otro tipo de hidrocarburos aromáticos se componen de sistemas aromáticos “condensados” o “anillos fusionados” los mas sencillos son el naftaleno, el antraceno, y el fenantreno No hay átomos de hidrógeno unidos a los átomos de carbono que intervienen en la fusión de anillos aromáticos esto es los átomos de carbono pertenecen a dos o mas anillos aromáticos.
Reacciones: oxidación y halogenación
Oxidación
- Los alcohilbencenos son fácilmente oxidables
- La oxidación no altera el núcleo bencénico y produce ácidos aromáticos cuyo carboxilo queda unido a un carbono del núcleo.
- El tolueno se oxida a acido benzoico
+3O -H 2 O
- Los xilenos a ácidos ftálicos por ejemplo el o-xileno da acido ortoftalico +6O -2H 2 O
Halogenación
La halogenación de los alcohilbencenos se hace por sustitución ya sea en el núcleo o en la cadena. De una manera general “la halogenación en el núcleo” se produce por la acción del halógeno en presencia de catalizador (limaduras de hierro, cloruro férrico, cloruro de aluminio, pentacloruro de antimonio) La “halogenación en cadena lateral” se logra por la acción directa del halógeno en ausencia de catalizador.
- Consiste en la introducción del grupo NITRO (-NO2)
- Sustituye: H, -SO3H,-OCH3,-CO-CH3 se obtienen derivados polinitrados
- Las nitraciones son exotérmica e irreversibles
- Los agentes nitrantes son: acido nítrico concentrado o el fumante
- Deshidratantes como: acido sulfúrico, óleum, anhídrido acético, pentoxido de fósforo * Nitratos alcalinos mas acido sulfúrico, nitraros orgánicos, nitratos metálicos mas acido acético, acido nitrosulfónico. Ar H + HO -NO2, Ar-NO2 + H2O
Nitrobenceno fenilamina +6H -2H2O Existe un enlace C-N que por reducción nos dan aminas primarias HIDROLISACION R –O—NO R–OH + HO.NO Nitrito de alcohol acido nitroso alcohilo Nitrobenceno HNO3, H2SO4 60°C HNO3, H2SO4 95°C NO 2 NO 2 NO 2 92% m- 7% o- 1% p-
Dinitrobencenos
Los nitrotolueno son utilizados en la fabricación de toluidas CH3-C6H4-NH2 que son materias primas en la industria de los colorantes. Se obtiene de la nitración del tolueno 2, 4, 6, -trinitrotolueno (o -TNT ) 2,3,4, -Trinitrotolueno ( o -TNT) 2,4,5, -trinitrotollueno (o y -TNT) TOLITA
Sulfonación
Consiste en la introducción del grupo –SO 3 H La reacción es reversible: OH Ar-H+SO 2 Ar-SO 3 H+H 2 O OH SO 2 Cl SO 2 NH 2 tolueno O-tolvensulfonilo O-toluensulfamina Acido o-sulfamidobenzoico sacarina CO OH So 2 NH H - H 2 O CO SO 2 NH En un medio ácido se obtiene anilina, en medio neutro fenilhidroxilamina en medio alcalino, hidrazobenceno Anilina hidrazobenceno Oxidación de anilina Se puede lograr de varias maneras El sulfato de anilina, en presencia de un gran exceso de ácido sulfúrico, se oxida a la temperatura ordinaria a quinona. La quinona es la reducción de la hidroquinona con el dióxido de azufre.
Fuente
- www.enciclonet.com
- www.textoscientificos.com
- www.slideshare.net