Diferencia entre revisiones de «Ley periódica»
| Línea 4: | Línea 4: | ||
|tamaño=301 × 238px- | |tamaño=301 × 238px- | ||
|concepto=<div align="justify">Compendió la variación gradual de las propiedades químicas de los elementos químicos a través de la '''Ley Periódica'''.</div> | |concepto=<div align="justify">Compendió la variación gradual de las propiedades químicas de los elementos químicos a través de la '''Ley Periódica'''.</div> | ||
| − | }}[[ | + | }}[[Ley Periódica|'''Ley Periódica''']] es la base de la tabla periódica y establece que las propiedades físicas y químicas de los elementos químicos tienden a repetirse de forma sistemática conforme aumenta el número atómico. |
== Desarrollo histórico == | == Desarrollo histórico == | ||
| Línea 23: | Línea 23: | ||
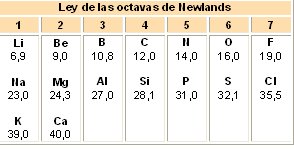
*Didimium, elemento conocido hasta 1885, que resultó ser una mezcla de praseodimio y neodimio.<br>Si bien el trabajo de Newlands fue incompleto, resultó de importancia, ya que puso en evidencia la estrecha relación existente entre los pesos atómicos de los elementos y sus propiedades físicas y químicas. | *Didimium, elemento conocido hasta 1885, que resultó ser una mezcla de praseodimio y neodimio.<br>Si bien el trabajo de Newlands fue incompleto, resultó de importancia, ya que puso en evidencia la estrecha relación existente entre los pesos atómicos de los elementos y sus propiedades físicas y químicas. | ||
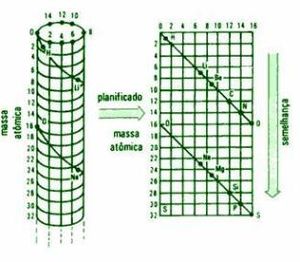
</div> <div align="justify"><br></div><div align="justify">En 1869, el profesor de Química Julius Lothar Meyer (1830-1895) [[Image:JMeyer.JPG|16x19px|to the side]] en la Universidad de Wroclaw cuando asistió al congreso de Karlsruhe. Las conclusiones del mismo le permitieron revisar las relaciones numéricas existentes entre los elementos químicos apoyándose en la teoría atómica de Dalton y la hipótesis de Avogadro. Basándose en estas nociones determinó los volúmenes atómicos de los elementos químicos, poniendo en evidencia una cierta periodicidad en el volumen atómico. Los elementos similares tienen un volumen atómico similar en relación con los otros elementos. Los metales alcalinos tienen por ejemplo un volumen atómico importante. </div> <div align="justify"><br></div><div align="justify">En 1869 habían muchas de las piezas del rompecabezas de los elementos químicos, el químico ruso [[Dimitri Ivanovich Mendeléiev]][[Image:DMendeleiev.JPG|16x18px|to the side]], era consciente del trabajo de Newlands, pero no le gustaba la manera en que lo expresaba. En particular, detestaba la forma en que algunos elementos parecían haber sido metidos con calzador para mantener la impresión de periodicidad. Él se dio cuenta de que clasificando los elementos según sus masas atómicas se veía aparecer una periodicidad en lo que concierne a ciertas propiedades de los elementos y que esas propiedades tenían que dar respuesta a una ley periódica que aun no se conocía. . </div> | </div> <div align="justify"><br></div><div align="justify">En 1869, el profesor de Química Julius Lothar Meyer (1830-1895) [[Image:JMeyer.JPG|16x19px|to the side]] en la Universidad de Wroclaw cuando asistió al congreso de Karlsruhe. Las conclusiones del mismo le permitieron revisar las relaciones numéricas existentes entre los elementos químicos apoyándose en la teoría atómica de Dalton y la hipótesis de Avogadro. Basándose en estas nociones determinó los volúmenes atómicos de los elementos químicos, poniendo en evidencia una cierta periodicidad en el volumen atómico. Los elementos similares tienen un volumen atómico similar en relación con los otros elementos. Los metales alcalinos tienen por ejemplo un volumen atómico importante. </div> <div align="justify"><br></div><div align="justify">En 1869 habían muchas de las piezas del rompecabezas de los elementos químicos, el químico ruso [[Dimitri Ivanovich Mendeléiev]][[Image:DMendeleiev.JPG|16x18px|to the side]], era consciente del trabajo de Newlands, pero no le gustaba la manera en que lo expresaba. En particular, detestaba la forma en que algunos elementos parecían haber sido metidos con calzador para mantener la impresión de periodicidad. Él se dio cuenta de que clasificando los elementos según sus masas atómicas se veía aparecer una periodicidad en lo que concierne a ciertas propiedades de los elementos y que esas propiedades tenían que dar respuesta a una ley periódica que aun no se conocía. . </div> | ||
| − | == '''Formulación | + | == '''Formulación ''' == |
=== ''' '''''Ley periódica de Mendeléiev'' === | === ''' '''''Ley periódica de Mendeléiev'' === | ||
| Línea 33: | Línea 33: | ||
El sistema periódico de los elementos es expresión de la ley periódica, [[Mendeléiev]], ordenó los elementos de acuerdo a su masa atómica y situó en una misma columna a aquellos que tenían algo en común. Su tabla, presentada en 1869, se basó en la variación manual de las propiedades químicas. La aceptación universal del la clasificación de Mendeleiev puede considerarse como un verdadero renacimiento del pensamiento químico. Por primera vez fueron relacionadas en un esquema lógico las variaciones de las propiedades de los elementos y sus compuestos, y dejó de ser necesario tratar un elemento como una individualidad totalmente desligada y sin relación con sus vecinos. La clave del éxito de sus esfuerzos fue comprender que los intentos anteriores habían fallado porque todavía quedaba un cierto número de elementos por descubrir, y había que dejar los huecos para esos elementos en la tabla. Por ejemplo, aunque no existía ningún elemento conocido hasta entonces con una masa atómica entre la del calcio(Ca) y la del titanio(Ti), [[Mendeléiev]] le dejó un sitio vacante en su sistema periódico. Este lugar fue asignado más tarde al elemento escandio, descubierto en 1879, que tiene unas propiedades que justifican su posición en esa secuencia. El descubrimiento del escandio sólo fue parte de una serie de verificaciones de las predicciones basadas en la ley periódica, y la validación del sistema periódico aceleró el desarrollo de la química inorgánica. | El sistema periódico de los elementos es expresión de la ley periódica, [[Mendeléiev]], ordenó los elementos de acuerdo a su masa atómica y situó en una misma columna a aquellos que tenían algo en común. Su tabla, presentada en 1869, se basó en la variación manual de las propiedades químicas. La aceptación universal del la clasificación de Mendeleiev puede considerarse como un verdadero renacimiento del pensamiento químico. Por primera vez fueron relacionadas en un esquema lógico las variaciones de las propiedades de los elementos y sus compuestos, y dejó de ser necesario tratar un elemento como una individualidad totalmente desligada y sin relación con sus vecinos. La clave del éxito de sus esfuerzos fue comprender que los intentos anteriores habían fallado porque todavía quedaba un cierto número de elementos por descubrir, y había que dejar los huecos para esos elementos en la tabla. Por ejemplo, aunque no existía ningún elemento conocido hasta entonces con una masa atómica entre la del calcio(Ca) y la del titanio(Ti), [[Mendeléiev]] le dejó un sitio vacante en su sistema periódico. Este lugar fue asignado más tarde al elemento escandio, descubierto en 1879, que tiene unas propiedades que justifican su posición en esa secuencia. El descubrimiento del escandio sólo fue parte de una serie de verificaciones de las predicciones basadas en la ley periódica, y la validación del sistema periódico aceleró el desarrollo de la química inorgánica. | ||
<div align="justify">El sistema periódico ha experimentado dos avances principales desde su formulación original por parte de Mendeléiev y Meyer</div> La primera revisión extendió el sistema para incluir toda una nueva familia de elementos cuya existencia era completamente insospechada en el siglo XIX. Este grupo comprendía los tres primeros elementos de los gases nobles o inertes, argón, helio y neón, descubiertos en la atmósfera entre 1894 y 1898 por el físico británico John William Strutt y el químico británico William Ramsay.;<br> El segundo avance fue la interpretación de la causa de la periodicidad de los elementos en términos de la teoría de Bohr (1913) sobre la estructura electrónica del átomo.;<br><div align="justify">Las bases de todo el desarrollo moderno de la química fueron sentadas en el periódo que siguió a la propuesta de [[Mendeléiev]] y al desarrollo sobre la estructura atómica.</div></div> | <div align="justify">El sistema periódico ha experimentado dos avances principales desde su formulación original por parte de Mendeléiev y Meyer</div> La primera revisión extendió el sistema para incluir toda una nueva familia de elementos cuya existencia era completamente insospechada en el siglo XIX. Este grupo comprendía los tres primeros elementos de los gases nobles o inertes, argón, helio y neón, descubiertos en la atmósfera entre 1894 y 1898 por el físico británico John William Strutt y el químico británico William Ramsay.;<br> El segundo avance fue la interpretación de la causa de la periodicidad de los elementos en términos de la teoría de Bohr (1913) sobre la estructura electrónica del átomo.;<br><div align="justify">Las bases de todo el desarrollo moderno de la química fueron sentadas en el periódo que siguió a la propuesta de [[Mendeléiev]] y al desarrollo sobre la estructura atómica.</div></div> | ||
| − | === | + | === Ley periódica moderna === |
<div align="justify">El sistema periódico como indicó [[Mendeléiev]], en 1889, no solo esperaba nuevas aplicaciones, sino también perfeccionamientos, un desarrollo minucioso y unas nuevas fuerzas científicas que lo impulsaran y añadió, en 1905, después de haber sido descubiertos los gases nobles “… a la ley periódica el futuro no lo amenaza con la destrucción, sino que solo promete superestructuras y desarrollo”. </div> <div align="justify"><br></div><div align="justify">Después de realizadas las correciones de masas atómicas y después del descubrimiento de nuevos elementos que fueron ocupando las casillas vacías de la tabla de Mendeliev, persistían, sin embargo, algunas anomalías en la tabla periódica.<br></div><div align="justify"><br></div><div align="justify">Por ejemplo:.;<br>a) El níquel (Ni), que se parece más al paladio (Pd) y al platino (Pt), y debe quedar en el mismo grupo, tiene una masa atómica menor que el cobalto (Co), no debiendo situarse antes que esté en la tabla..;<br>b) El argón (Ar), que pertenece por sus propiedades al grupo de los gases nobles, tiene una masa atómica superior a la del potasio (K) que debe seguirle en orden sucesivo en la tabla..;<br>c) El teluro (Tl) que tiene una masa atómica superior al yodo (I) es muy semejante al azufre (S) y al selenio (Se), y debe estar antes que el yodo para encajar en el grupo del oxígeno (O). </div> <div align="justify"><br></div><div align="justify">De acuerdo con todo esto se hizo evidente que la masa atómica creciente es un criterio de ordenamiento imperfecto para la estructuración de la tabla periódica.</div> <div align="justify"><br></div><div align="justify">Realmente las causas de estas anomalías están en que las masas atómicas son las masas promedio de las mezclas de isótopos que constituyen cada elemento y están en relación con las cantidades relativas de cada clase de átomo en la mezcla isotópica. Es decir, que la masa atómica no es una propiedad de clase de átomo, sino del elemento o conjunto de átomos de igual carga nuclear.</div> | <div align="justify">El sistema periódico como indicó [[Mendeléiev]], en 1889, no solo esperaba nuevas aplicaciones, sino también perfeccionamientos, un desarrollo minucioso y unas nuevas fuerzas científicas que lo impulsaran y añadió, en 1905, después de haber sido descubiertos los gases nobles “… a la ley periódica el futuro no lo amenaza con la destrucción, sino que solo promete superestructuras y desarrollo”. </div> <div align="justify"><br></div><div align="justify">Después de realizadas las correciones de masas atómicas y después del descubrimiento de nuevos elementos que fueron ocupando las casillas vacías de la tabla de Mendeliev, persistían, sin embargo, algunas anomalías en la tabla periódica.<br></div><div align="justify"><br></div><div align="justify">Por ejemplo:.;<br>a) El níquel (Ni), que se parece más al paladio (Pd) y al platino (Pt), y debe quedar en el mismo grupo, tiene una masa atómica menor que el cobalto (Co), no debiendo situarse antes que esté en la tabla..;<br>b) El argón (Ar), que pertenece por sus propiedades al grupo de los gases nobles, tiene una masa atómica superior a la del potasio (K) que debe seguirle en orden sucesivo en la tabla..;<br>c) El teluro (Tl) que tiene una masa atómica superior al yodo (I) es muy semejante al azufre (S) y al selenio (Se), y debe estar antes que el yodo para encajar en el grupo del oxígeno (O). </div> <div align="justify"><br></div><div align="justify">De acuerdo con todo esto se hizo evidente que la masa atómica creciente es un criterio de ordenamiento imperfecto para la estructuración de la tabla periódica.</div> <div align="justify"><br></div><div align="justify">Realmente las causas de estas anomalías están en que las masas atómicas son las masas promedio de las mezclas de isótopos que constituyen cada elemento y están en relación con las cantidades relativas de cada clase de átomo en la mezcla isotópica. Es decir, que la masa atómica no es una propiedad de clase de átomo, sino del elemento o conjunto de átomos de igual carga nuclear.</div> | ||
La masa atómica depende de la abundancia de cada isótopo en la mezcla y varía de acuerdo con esto para cada elemento. | La masa atómica depende de la abundancia de cada isótopo en la mezcla y varía de acuerdo con esto para cada elemento. | ||
| Línea 43: | Línea 43: | ||
'''“Las propiedades físicas y químicas de los elementos son funciones de las configuraciones eslectrónicas de sus átomos, las cuales varían periódicamente al aumentar el número atómico”''', postulado conocido como la Ley periódica de Moseley. Es decir, las propiedades de los elementos varían periódicamente cuando se ordenan según sus cargas nucleares y cada cierto número de elementos las propiedades se repiten. | '''“Las propiedades físicas y químicas de los elementos son funciones de las configuraciones eslectrónicas de sus átomos, las cuales varían periódicamente al aumentar el número atómico”''', postulado conocido como la Ley periódica de Moseley. Es decir, las propiedades de los elementos varían periódicamente cuando se ordenan según sus cargas nucleares y cada cierto número de elementos las propiedades se repiten. | ||
| − | + | <br> | |
== Referencias <br> == | == Referencias <br> == | ||
Revisión del 18:46 12 may 2011
| ||||||
Ley Periódica es la base de la tabla periódica y establece que las propiedades físicas y químicas de los elementos químicos tienden a repetirse de forma sistemática conforme aumenta el número atómico.
Sumario
Desarrollo histórico
Primeros intentos de clasificaciones de los elementos químicos
La semejanza de las propiedades físicas y químicas de ciertos elementos sugirió a los científicos del siglo XIX la posibilidad de ordenarlos sistemáticamente o agruparlos de a acuerdo con determinado criterio. Johann Wolfgang Döbereiner (1780-1849) to the side
Ca - Sr – Ba, S - Se – Te, Li - Na - K
La importancia del trabajo de Döbereiner radica en que fue el 1° intento de clasificación de los elementos. En su época eran muy pocos los elementos conocidos y los valores de los pesos atómicos todavía estaban en discusión.
- Glucinium o glucinum es el berilio.
- Didimium, elemento conocido hasta 1885, que resultó ser una mezcla de praseodimio y neodimio.
Si bien el trabajo de Newlands fue incompleto, resultó de importancia, ya que puso en evidencia la estrecha relación existente entre los pesos atómicos de los elementos y sus propiedades físicas y químicas.
Formulación
Ley periódica de Mendeléiev
Mendeléiev estudió el cambio las propiedades químicas de las sustancias en función del crecimiento de las masas atómicas de los elementos químicos, y analizó el comportamiento de la valencia de los elementos químicos, las propiedades y composición de los compuestos que estos forman.
El sistema periódico de los elementos es expresión de la ley periódica, Mendeléiev, ordenó los elementos de acuerdo a su masa atómica y situó en una misma columna a aquellos que tenían algo en común. Su tabla, presentada en 1869, se basó en la variación manual de las propiedades químicas. La aceptación universal del la clasificación de Mendeleiev puede considerarse como un verdadero renacimiento del pensamiento químico. Por primera vez fueron relacionadas en un esquema lógico las variaciones de las propiedades de los elementos y sus compuestos, y dejó de ser necesario tratar un elemento como una individualidad totalmente desligada y sin relación con sus vecinos. La clave del éxito de sus esfuerzos fue comprender que los intentos anteriores habían fallado porque todavía quedaba un cierto número de elementos por descubrir, y había que dejar los huecos para esos elementos en la tabla. Por ejemplo, aunque no existía ningún elemento conocido hasta entonces con una masa atómica entre la del calcio(Ca) y la del titanio(Ti), Mendeléiev le dejó un sitio vacante en su sistema periódico. Este lugar fue asignado más tarde al elemento escandio, descubierto en 1879, que tiene unas propiedades que justifican su posición en esa secuencia. El descubrimiento del escandio sólo fue parte de una serie de verificaciones de las predicciones basadas en la ley periódica, y la validación del sistema periódico aceleró el desarrollo de la química inorgánica.
El segundo avance fue la interpretación de la causa de la periodicidad de los elementos en términos de la teoría de Bohr (1913) sobre la estructura electrónica del átomo.;
Ley periódica moderna
a) El níquel (Ni), que se parece más al paladio (Pd) y al platino (Pt), y debe quedar en el mismo grupo, tiene una masa atómica menor que el cobalto (Co), no debiendo situarse antes que esté en la tabla..;
b) El argón (Ar), que pertenece por sus propiedades al grupo de los gases nobles, tiene una masa atómica superior a la del potasio (K) que debe seguirle en orden sucesivo en la tabla..;
c) El teluro (Tl) que tiene una masa atómica superior al yodo (I) es muy semejante al azufre (S) y al selenio (Se), y debe estar antes que el yodo para encajar en el grupo del oxígeno (O).
La masa atómica depende de la abundancia de cada isótopo en la mezcla y varía de acuerdo con esto para cada elemento.
Donde σ y C son constantes que dependen del tipo de serie de espectros. A la ecuación anterior se le denomina ley de Moseley.
“Las propiedades físicas y químicas de los elementos son funciones de las configuraciones eslectrónicas de sus átomos, las cuales varían periódicamente al aumentar el número atómico”, postulado conocido como la Ley periódica de Moseley. Es decir, las propiedades de los elementos varían periódicamente cuando se ordenan según sus cargas nucleares y cada cierto número de elementos las propiedades se repiten.
Referencias
- Lara Piñeiro. A.R. E. Calero Martín y J. Labadié Suárez: Materiales Complementarios de Química para Ingenieros. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1987.
- León Ramírez, R.: Química General. Ed. Pueblo y Educación. Ciudad de La Habana, Cuba. 1985
Fuentes
- http://www.fq.uh.cu/dpto/qf/uclv/infoLab/infoquim/asig_programs/prog.lic.quimica/temas/estruc_atom_ley_period.htm
- http://quimica-general.net16.net/ley_periodica.html
- http://www.xtec.cat/~bnavarr1/Tabla/castellano/moseley.htm
Enlaces externos