Hemofilia B
| ||||||
Hemofilia B. Técnicas coagulométricas e inmunológicas han permitido identificar diferentes variantes moleculares. En la mayoría de los enfermos la gravedad clínica de la hemofilia B está relacionada con las tasas funcionales de factor IX, no con el material antigénico circulante.
Sumario
Prevalencia y genética
Al igual que la hemofilia A, el déficit congénito de factor IX se presenta en todas las etnias, aunque con una incidencia menor; así, aproximadamente, el número de casos de hemofilia B corresponde a la tercera parte de los de hemofilia A.
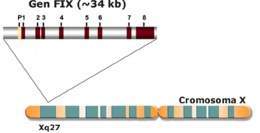
También es un trastorno recesivo ligado al cromosoma X, y el gen del factor IX se encuentra en un fragmento del 34 kb, localizado en su brazo largo. La hemofilia B es una enfermedad heterogénea en cuanto a su origen. Las deleciones parciales o completas del gen representan el principal defecto molecular responsable de la hemofilia B. Por lo general estos defectos son fácilmente identificables con enzimas de restricción. La existencia de mutaciones puntuales es la responsable de las formas variantes de enfermedad (alteraciones funcionales). Se han identificado un importante número de alteraciones moleculares responsables de la hemofilia B.
Cuadro clínico
Las manifestaciones hemorrágicas en la hemofilia B son indistinguibles de las observadas en los pacientes con hemofilia A. La gravedad del cuadro hemorrágico está relacionada con la actividad funcional del factor IX circulante, por lo que los criterios de clasificación de la enfermedad son los referidos para la hemofilia A.
Diagnóstico
Se usan criterios diagnósticos similares a los utilizados en la hemofilia A, si bien en este caso el factor deficitario es el IX. Es recomendable utilizar una tromboplastina de buey para clasificar definitivamente la deficiencia. Al igual que en la hemofilia A, la utilización de sondas de DNA facilitará la identificación de las portadoras y el diagnóstico prenatal de la enfermedad.
Diagnóstico diferencial
Clínicamente la hemofilia B no puede distinguirse de la hemofilia A. La dosificación de los factores permite identificar el problema. La disminución adquirida del factor IX se acompaña de un defecto de los restantes factores dependientes de la vitamina K. Existe una rara deficiencia congénita en la que se encuentra un déficit combinado de los factores II, VII, IX y X y de las proteínas C y S, debido a un trastorno de la gammacarboxilación de las proteínas dependientes de la vitamina K.
Tratamiento
Es similar al señalado para la hemofilia A. En este caso, los productos que se han de utilizar son los concentrados plasmáticos, previamente sometidos a inactivación vírica, de complejo protrombínico (mezcla de factores II, VII, IX y X) o concentrados específicos de factor IX. Éste presenta una farmacocinética diferente a la del factor VIII, de ahí que las recomendaciones terapéuticas difieran de las pautas establecidas para la hemofilia A. Dado que los concentrados plasmáticos de complejo protrombínico pueden tener actividad trombogénica, se aconseja utilizar preparados purificados específicos de factor IX. El uso de 25-50 U/kg de factor IX suele ser suficiente para alcanzar una buena hemostasia. Dado que la vida media del factor IX es de unas 20 h, aproximadamente, se pueden aconsejar perfusiones del preparado cada 12 o 24 h. Recientemente, se pueden utilizar preparados de factor IX recombinante, habiéndose demostrado su eficacia y seguridad terapeútica.
Complicaciones del tratamiento
Las complicaciones de la hemofilia B son las mismas que se han señalado en los hemofílicos A. Sólo cabe indicar que la prevalencia de inhibidores contra el factor IX en los hemofílicos B politransfundidos es del 5%.
Fuente
• Ciril Ferreras Rozman, Medicina Interna, Ediciones Harcourt, 14 Edición, 2000.
• Escribano L, Orfao A, Díaz Agustín B, Villarrubia J, Cerveró C, López A et al. Indolent systemic mast cell disease in adults. Immunophenotypic characterization and its diagnostic implications. Blood 1997; 91:2731-2736.
• Escribano L, Villarrubia J, Cerveró C, Bellas C. Mastocitosis sistémica. Clasificación, clínica, diagnóstico y tratamiento. Medicine (Madr) 1996; 7:1367-1372.
• Golkar L, Bernhard JD. Mastocytosis. Lancet 1997; 349:1379-1385.
• Horny HP, Ruck P, Krober S, Kaiserling E. Systemic mast cell disease (mastocytosis). General aspects and histopathological diagnosis. Histol Histopathol 1997; 12:1081-1089.