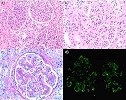
Macroglobulinemia de Waldenström
| ||||
Sumario
Definición
La macroglobulinemia de Waldenström (MW) es una neoplasia de la célula B caracterizada por un infiltrado linfoplasmocítico de la médula ósea, asociado a la presencia de una paraproteína monoclonal de clase IgM, misma que se encuentra en el plasma en una alta concentración. En su descripción original de 1944, Waldenström informó de dos pacientes con hemorragia oronasal, linfadenopatía, tasa de sedimentación alta, hiperviscosidad, frotis de sangre periférica normal, citopenias y un infiltrado de predominio linfoide en la médula ósea. La macroglobulinemia de Waldenström se define en la actualidad como un linfoma linfoplasmocítico (LPL) en la clasificación revisada europeoamericana de linfomas (REAL, Revised Euro American Lymphoma, por sus siglas en inglés).
Etiopatogenia
El origen de la macroglobulinemia de Waldenström se desconoce; sin embargo, hay algunos informes que la han asociado con la exposición a radiaciones ionizantes y a la infección por el virus de la hepatitis C; también se han descrito anormalidades citogenéticas, aunque no hay alguna que sea característica de esta enfermedad. En muchos de los pacientes, la presencia de la IgM anormal induce trastornos serios de la coagulación, con alteración en la agregabilidad plaquetaria, por lo cual la hemorragia es una de las principales manifestaciones. Con respecto a la célula de origen, no se ha identificado de manera precisa, aunque los datos señalan al linfocito T de memoria. Las células en la MW expresan niveles altos de interleucina 6 (IL-6), lo que concuerda con las cifras altas en suero de la proteína C reactiva que se suele encontrar en estos casos.
Cuadro clínico
Los síntomas se pueden dividir en dos tipos: los asociados a la proliferación clonal e infiltración tumoral de la médula ósea, y los debidos al efecto reológico de la macroglobulina monoclonal. Las manifestaciones más comunes son debilidad, fatiga y pérdida de peso, además de hemorragia en mucosas y articulaciones; la anemia puede resultar de la infi ltración de la médula ósea, hemólisis autoinmune y niveles altos de IL-6, que se ven refl ejados en un incremento de la proteína C reactiva, así como de la producción disminuida de eritropoyetina. La trombocitopenia puede resultar de la misma infi ltración tumoral, del desarrollo de una púrpura trombocitopénica inmune(PTI), o ser secundaria a esplenomegalia. Las manifestaciones de hiperviscosidad más frecuentes son la cefalea, vértigo, visión borrosa y neuropatía periférica, principalmente de tipo sensitivo. Las anormalidades neurológicas en la MW se conocen como síndrome de Bing-Neel. En caso de haber manifestaciones neurológicas focales o globales que puedan deberse a hiperviscosidad se debe proceder a una plasmaféresis de inmediato; los síntomas pueden ser inespecíficos, como fatiga, confusión, desarrollo de un accidente cerebrovascular, alteraciones cognitivas y, en casos extremos, demencia franca. Sin embargo, lo más frecuente son los síntomas moderados, como la cefalea persistente. Como consecuencia directa de la hiperviscosidad, en la retina pueden presentarse exudados cotonoides, ingurgitación venosa y hemorragias visibles en el examen del fondo ocular. En los casos más graves puede producirse la oclusión de la vena central de la retina. Datos de una neuropatía periférica pueden encontrarse hasta en el 20% de los pacientes con MW, debido a la acción de la IgM actuando como un autoanticuerpo contra antígenos localizados en la capa de mielina. La manifestación más común es la neuropatía crónica desmielinizante, distal y simétrica, con défi cit sensitivos y de la propiocepción, lo que resulta en ataxia; en estos casos, se encuentran anticuerpos dirigidos contra las glicoproteínas asociadas a la mielina. Otras causas de neuropatía que deben descartarse en los individuos con MW son la deficiencia de vitamina B 12 , la presencia de crioglobulinas y la amiloidosis. Los hallazgos físicos más comunes son hepatomegalia en el 20% de los casos y esplenomegalia en el 15%. La linfadenopatía, por su parte, es detectable en 15 a 20% de los pacientes; en ocasiones, se observa el fenómeno de Raynaud en las extremidades.
Diagnóstico diferencial
No hay características morfológicas, genéticas o inmunofenotípicas específicas de la MW, por lo que es difícil distinguirla de enfermedades similares, lo que se complica además por la superposición de los datos. En el diagnóstico diferencial, deben contemplarse otras neoplasias de la célula B, como el linfoma de la célula del manto, la leucemia linfocítica crónica de célula B, el linfoma linfocítico de células pequeñas, el linfoma folicular, el linfoma de la zona marginal y el mieloma múltiple, así como la amiloidosis y enfermedades autoinmunes. La entidad más difícil de diferenciar es el linfoma linfoplasmocitoide. Resulta importante distinguir el MW de la gammapatía monoclonal de significado indeterminado (MGUS), pues hay notables diferencias en el pronóstico correspondiente. Por ejemplo, los individuos con < 10% de infi ltración de la médula ósea y < 3 g/dl de IgM en suero (MGUS IgM) tienen un riesgo de progresión hacia la enfermedad sintomática de sólo 1.5% por año, en tanto que la MW sintomática conlleva una tasa de mortalidad cinco veces mayor a la de la población general. Resulta relevante descartar la presencia de amiloidosis asociada a la MW, sobre todo la pleural y la pulmonar, debido al mal pronóstico asociado en estos casos y a que cualquier neoplasia productora de una proteína monoclonal puede complicarse con la presencia concurrente de amiloidosis.
Tratamiento
La decisión de dar tratamiento depende de la presencia de síntomas de hiperviscosidad, adenopatía significativa, organomegalia importante, neuropatía, síntomas constitucionales, presencia de amiloidosis general, transformación a linfoma de alto grado, presencia de enfermedad por crioaglutininas, crioglobulinemia sintomática o sospecha de daño orgánico. Las citopenias sintomáticas, sobre todo una Hb < 10 g/dl, también constituyen una base suficiente para iniciar el tratamiento. Por el contrario, la concentración sérica de la IgM y el tamaño del pico monoclonal no deben ser los únicos criterios que se consideren para iniciar el tratamiento. En la enfermedad asintomática, sólo es necesaria la observación frecuente del paciente; en la MW temprana se debe considerar el administrar el anticuerpo monoclonal rituximab, como único tratamiento; en la MW avanzada es necesario agregar al rituximab un alquilante o un análogo de los nucleósidos de las purinas. En ausencia de rituximab o la fludarabina, deben usarse elclorambucilo, la ciclofosfamida o la 5-clorodesoxiadenosina, ya que no hay datos suficientes para recomendar la administración de un medicamento de primera línea sobre otro, e incluso en individuos seleccionados hay que considerar un trasplante de progenitores hematopoyéticos. Es pertinente notar que la terapia en la que se combinan distintos medicamentos, aunque obtiene una más rápida disminución de la masa tumoral, tiene como contraparte la suma de los efectos tóxicos de los agentes administrados, sin haberse demostrado claramente la superioridad a largo plazo de esta modalidad sobre el tratamiento con monoterapia. Los lineamientos más recientes para la clasificación y selección del tratamiento. Si los síntomas secundarios a hiperviscosidad son clínicamente significativos, debe someterse al paciente a plasmaféresis terapéutica, retirando de uno a uno y medio volúmenes plasmáticos, calculando éste a 40 ml/kg de peso corporal, reponiendo el plasma retirado con una solución de albúmina al 5% en solución salina normal. Por lo general, se logra una buena respuesta, aunque la plasmaféresis en sí misma no es curativa ni tiene efecto alguno sobre la masa tumoral, por lo que de manera simultánea debe iniciarse la quimioterapia. Fármacos adicionales que están siendo estudiados clínicamente son el bortezomib, la talidomida, el sildenafilo y el oblimersen, entre otros, con resultados variables y sin haber demostrado su superioridad sobre los medicamentos ya mencionados.
Fuentes
- https://www.fcarreras.org/es/macroglobulinemia-de-waldenstrom_370111
- https://www.mayoclinic.org/es-es/.../waldenstrom-macroglobulinemia/.../syc-2035996...
- https://www.cancerdelasangre.com/soy-paciente/macroglobulinemia-de-waldenstrom/
- https://www.mdanderson.es/cancer/macroglobulinemia-de-waldenstrom