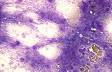
Trombocitemia esencial
| ||||||
Trombocitemia esencial. La trombocitemia esencial es actualmente el más frecuente de los SMPC (40% de la casuística del autor). Predomina en sujetos de 50 a 80 años, aunque una cuarta parte tienen menos de 35 años y pueden verse casos en la infancia. Es más frecuente en mujeres. Al no existir marcador para esta enfermedad, su diagnóstico obliga a descartar los restantes SMPC y otras causas de trombocitosis secundaria.
Sumario
Cuadro clínico
La práctica generalizada de exámenes de revisión ha hecho que cada vez sean más frecuentes las formas asintomáticas, que en algunas series constituyen hasta el 60% de los casos. La sintomatología más común se debe a trastornos en la microcirculación (dolores isquémicos en los dedos de los pies o en las plantas y palmas –eritromelalgia–, acrocianosis, parestesias, cefalea pulsátil, vértigo, acúfenos).
Son menos habituales las trombosis arteriales o venosas de vasos de mayor calibre (infarto cerebral, de miocardio o mesentérico, trombosis venosa de extremidades inferiores, embolia pulmonar, trombosis portal o esplénica).
Las complicaciones hemorrágicas (cutaneomucosas, gastrointestinales, metrorragias) son menos frecuentes. En la exploración física se detecta una ligera esplenomegalia en menos del 20% de los casos y más raramente hepatomegalia.
Datos de laboratorio
Destaca la trombocitosis superior a 600 109/L. Las plaquetas tienen una morfología anormal, con anisocitosis y formas gigantes, así como anomalías en su función, lo que explica la tendencia al sangrado. La cifra de leucocitos es normal o existe una ligera leucocitosis neutrofílica, rara vez con basofilia o ligera mielemia. La hemoglobina suele ser normal, así como la actividad de la FAG, y puede haber un ligero aumento de LDH y vitamina B12 séricas.
El aspirado medular pone de manifiesto una celularidad normal o algo aumentada, con hiperplasia de los megacariocitos, que en ocasiones son grandes y de núcleo hipersegmentado y en otras tienen un aspecto hipoploide. En el examen ultraestructural los megacariocitos presentan grandes oquedades citoplasmáticas y perinucleares.
El hierro medular suele estar disminuido, si bien ello no suele reflejar una auténtica ferropenia, pues la ferritinemia casi siempre es normal. En la biopsia medular destacan la conservación de la grasa y la hiperplasia de los megacariocitos que tienden a formar pequeños grupos, y a veces existe fibrosis reticulínica, por lo general moderada.
Diagnóstico
El diagnóstico de trombocitemia esencial es de exclusión. En la actualidad se utilizan los criterios establecidos por el Polycythemia Vera Study Group:
a) cifra de plaquetas superior a 600 109/L, comprobada al menos en dos ocasiones.
b) ausencia de causas potencialmente inductoras de trombocitosis (ferropenia –demostrada mediante el estudio de la ferritinemia, neoplasia, infección, enfermedad inflamatoria crónica, esplenectomía u otras).
c) normalidad del volumen eritrocitario determinado con métodos isotópicos (si la cifra de hemoglobina es superior a 130 g/L).
d) ausencia de fibrosis colágena en la médula ósea (en caso de fibrosis reticulínica intensa no deben existir datos sugestivos de mielofibrosis idiopática).
e) ausencia del cromosoma Ph o de reordenamiento BCR/ABL.
f) ausencia de signos citológicos o citogenéticos (5q–) de mielodisplasia.
Evolución y pronóstico
Con las medidas terapéuticas actuales la supervivencia de los pacientes con trombocitemia no difiere de la de la población general. Las complicaciones vasculares constituyen una causa frecuente de morbilidad, pero rara vez causan la muerte. Es rara la evolución a leucemia aguda, la mayoría de las veces en pacientes tratados con 32P o agentes alquilantes. También puede observarse la evolución a mielofibrosis.
Tratamiento
En el tratamiento de esta enfermedad debe sopesarse la necesidad de prevenir las complicaciones trombóticas o hemorrágicas frente al peligro de iatrogenia (en especial, leucemia aguda). Por ello, hay que valorar cuatro aspectos: edad del paciente, antecedentes trombóticos, existencia de sintomatología y factores de riesgo vascular.
En los enfermos mayores de 75 años el 32P es la terapéutica de elección, mientras que la hidroxiurea lo es de los 60 a los 75 años. Si los pacientes tienen menos de 60 años, se hallan asintomáticos y carecen de factores de riesgo vascular (hipertensión arterial, diabetes, hiperlipemia) o antecedentes isquémicos (ángor, infarto de miocardio, trombosis cerebral o de otros territorios, embolia pulmonar) cabe la abstención terapéutica, realizando sólo revisiones periódicas.
En enfermos de esa edad sin factores de riesgo vascular pero con sintomatología de escasa relevancia clínica (parestesias, cefaleas esporádicas, eritromelalgia) pueden administrarse fármacos antiagregantes plaquetarios en pequeñas dosis (ácido acetilsalicílico, 100-150 mg/día). En individuos menores de 60 años con trombosis, sintomatología más intensa o factores de riesgo vascular, la hidroxiurea es el tratamiento de elección, excepto por debajo de los 50 años, en que está indicado el anagrelide, por su ausencia de potencial leucemógeno. La trombocitoaféresis puede ser útil para reducir las plaquetas de forma rápida si la situación clínica lo requiere. Los fármacos antiagregantes (ácido acetilsalicílico, dipiridamol) en pequeñas dosis pueden administrarse a los pacientes con isquemia cerebral, coronaria o periférica. Es necesario eliminar el hábito tabáquico.
Fuente
- Ciril Ferreras Rozman, Medicina Interna, Ediciones Harcourt, 14 Edición, 2000.
- Escribano L, Orfao A, Díaz Agustín B, Villarrubia J, Cerveró C, López A et al. Indolent systemic mast cell disease in adults. Immunophenotypic characterization and its diagnostic implications. Blood 1997; 91:2731-2736.
- Escribano L, Villarrubia J, Cerveró C, Bellas C. Mastocitosis sistémica. Clasificación, clínica, diagnóstico y tratamiento. Medicine (Madr) 1996; 7:1367-1372.
- Golkar L, Bernhard JD. Mastocytosis. Lancet 1997; 349:1379-1385.
- Horny HP, Ruck P, Krober S, Kaiserling E. Systemic mast cell disease (mastocytosis). General aspects and histopathological diagnosis. Histol Histopathol 1997; 12:1081-1089.